製造業の品質管理において欠かせない書類のひとつが「検査成績書」です。製品の品質を証明し、取引先との信頼関係を支える重要な書類ですが、その作成・管理方法に課題を抱えている企業は少なくありません。紙ベースでの運用による保管スペースの問題、検索性の低さ、そして改ざんリスクなど、現場が直面する悩みは多岐にわたります。
本記事では、検査成績書の基本的な定義から記載内容、関連書類との違い、運用上の課題、そして電子化のメリットとシステム選定のポイントまでをわかりやすく解説します。品質管理体制の改善や業務効率化をお考えの方は、ぜひ参考にしてください。
目次
検査成績書の基本理解
検査成績書とは何か
検査成績書とは、製品や部品に対して実施した検査・試験の結果をまとめた書類です。英語では「Inspection Certificate」や「Test Report」と呼ばれ、「けんさせいせきしょ」と読みます。製造業を中心に幅広い業界で使用されており、製品が所定の規格や仕様を満たしていることを客観的なデータで証明する役割を担っています。
検査成績書には、寸法測定、強度試験、外観検査など、製品ごとに定められた検査項目の結果が数値データとともに記録されます。製造業だけでなく、建設業、食品業界、医薬品業界など、品質保証が重要視されるあらゆる分野で活用されています。出荷前の品質確認として作成されることが多く、納品時に取引先へ提出することで、製品の品質保証を行います。
検査成績書の目的と役割
検査成績書の最も重要な目的は、製品の品質を客観的に証明することです。検査結果を数値として記録し、規格値や基準値との合否判定を明示することで、製品が求められる品質基準を満たしていることを示します。
また、検査成績書はトレーサビリティ(追跡可能性)の確保にも重要な役割を果たします。万が一、製品に不具合が発生した場合、検査成績書を遡ることで製造ロットや検査時点の状態を特定でき、原因究明や迅速な対応が可能になります。品質管理の方針として、検査成績書の適切な作成・保管を徹底している企業は多く、取引先や業界全体からの信頼性向上にもつながります。
検査成績書の主な記載内容
検査成績書に記載される主な項目は以下のとおりです。
検査成績書の上部には、発行者情報(会社名・部署名)、発行日(年月日)、文書番号が記載されます。次に、検査対象の情報として、製品名称、型番・品番、製造ロット番号、数量、材料の種類や規格などが明記されます。
検査結果の項目としては、検査項目名(寸法、重量、硬度、引張強度、外観など)、検査方法(ノギス、マイクロメーター等の計測機器の種類を含む)、規格値・基準値、実測値(測定データ)、そして合格・不合格の判定結果が記載されます。
最後に、検査担当者名、承認者名、検査日が記録され、必要に応じて備考欄に特記事項や参考情報が加えられます。これらの項目を漏れなく正確に記載することが、検査成績書の信頼性を担保するポイントです。
検査成績書と関連書類の違い
ミルシートとの違い
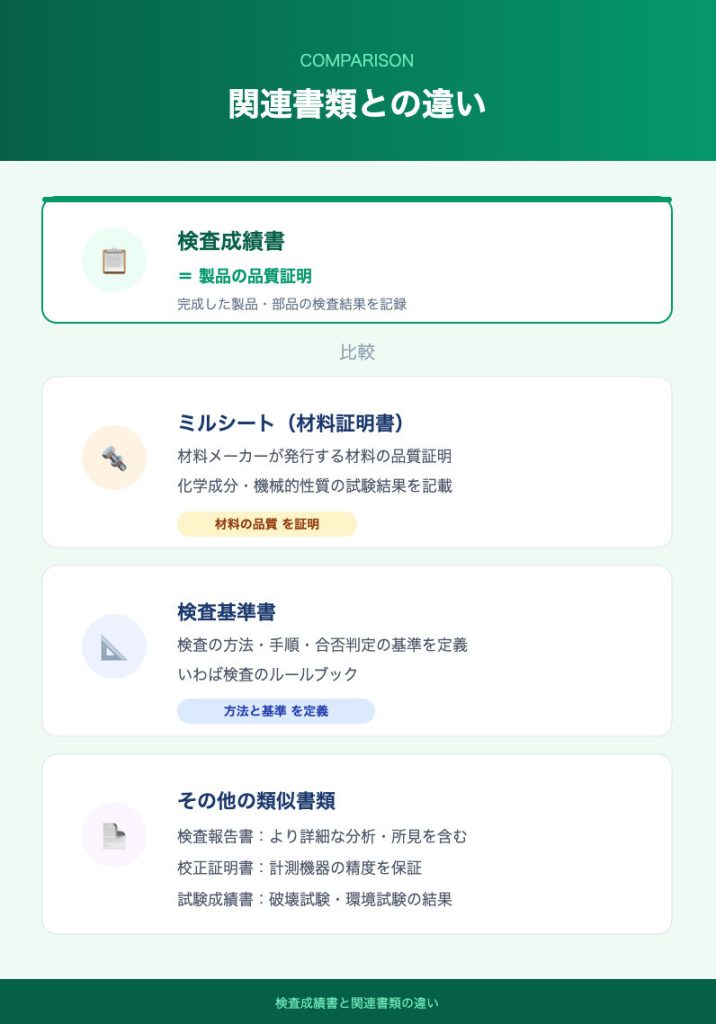
検査成績書とミルシートは混同されやすい書類ですが、目的と記載内容に明確な違いがあります。
ミルシート(材料証明書)は、鋼材をはじめとする材料のメーカーが発行する書類で、材料の化学成分や機械的性質(引張強度、降伏点など)の試験結果が記載されています。材料そのものの品質を証明するための書類です。
一方、検査成績書は完成した製品や部品に対する検査結果を記録する書類であり、寸法検査や外観検査など、製品としての品質を証明するものです。つまり、ミルシートは「材料の品質証明」、検査成績書は「製品の品質証明」という違いがあります。実際の取引では、材料段階のミルシートと製品段階の検査成績書の両方が求められるケースも多いです。
検査基準書との違い
検査基準書は、検査の方法・手順・合否判定の基準を定めた文書です。いわば検査のルールブックであり、「どのように検査を行うべきか」を示す規格文書です。
対して検査成績書は、検査基準書に基づいて実際に検査を行った「結果」を記録する書類です。検査基準書が「方法と基準」を定義するのに対し、検査成績書は「実際の測定値と判定結果」を報告するという関係にあります。
検査成績書と類似書類の違い
検査成績書と混同されやすい書類には、検査基準書やミルシートのほかにも複数あります。検査報告書は検査成績書とほぼ同義で使われることが多いですが、より詳細な分析や所見を含むケースもあります。校正証明書は計測機器の精度を保証する書類であり、検査成績書の信頼性を間接的に支える役割があります。試験成績書も検査成績書と類似していますが、試験成績書は特に破壊試験や環境試験などの結果を記録する場合に用いられることが多い点が異なります。
検査成績書の運用と管理
検査成績書の作成と管理方法
検査成績書の作成方法は企業によって異なりますが、一般的にはExcelなどの表計算ソフトで作成するケースが多く見られます。あらかじめフォーマットを用意しておき、検査担当者が測定値を入力して合否判定を行い、承認者の確認を経て発行するという流れが標準的です。近年では、計測機器から測定データを自動取り込みし、検査成績書を自動生成するシステムを導入する企業も増えています。
管理方法としては、紙に印刷してファイリングする方法と、電子データとして保管する方法があります。品質マネジメントシステム(ISO 9001等)を取得している企業では、記録の管理手順が明確に定められており、保存期間や保管場所、アクセス権限などが規定されています。いずれの方法でも、検査成績書が必要な時にすぐに取り出せる状態を維持しておくことが、品質管理の基本です。
紙ベース運用の課題
紙ベースでの検査成績書の管理には、多くの課題が存在します。
まず、物理的な保管スペースの問題です。製造業では製品ごとに検査成績書を発行するため、年間で膨大な量の書類が発生します。保管場所の確保やファイリングの手間は、現場にとって大きな負担です。
次に、検索性の低さが挙げられます。過去の検査成績書を参照したい場合、紙の書類を1枚ずつ探す必要があり、多大な時間と工数がかかります。不具合発生時に迅速なトレーサビリティが求められる場面では、この検索の遅れが品質管理上の深刻な問題につながります。
さらに、紛失や劣化のリスクも見逃せません。紙は経年劣化するうえ、火災や水害による消失の危険もあります。手書きの場合は記載ミスや転記漏れが発生しやすく、品質データの正確性にも影響を及ぼします。
加えて、紙の検査成績書はPDFデータと同様に改ざんのリスクがあります。数値の書き換えやすり替えが行われても検知が困難であり、品質偽装につながる可能性があります。
電子化のメリットと事例
検査成績書の電子化には、紙ベース運用の課題を解決する多くのメリットがあります。
データの一括管理と検索性の向上により、必要な検査成績書を瞬時に検索・参照できるようになります。製品名やロット番号、検査日などのキーワードで検索できるため、トレーサビリティの確保が格段に容易になります。保管スペースの削減、バックアップによるデータ消失リスクの軽減、入力作業の効率化とヒューマンエラーの防止など、業務効率の向上とコスト削減が同時に実現します。
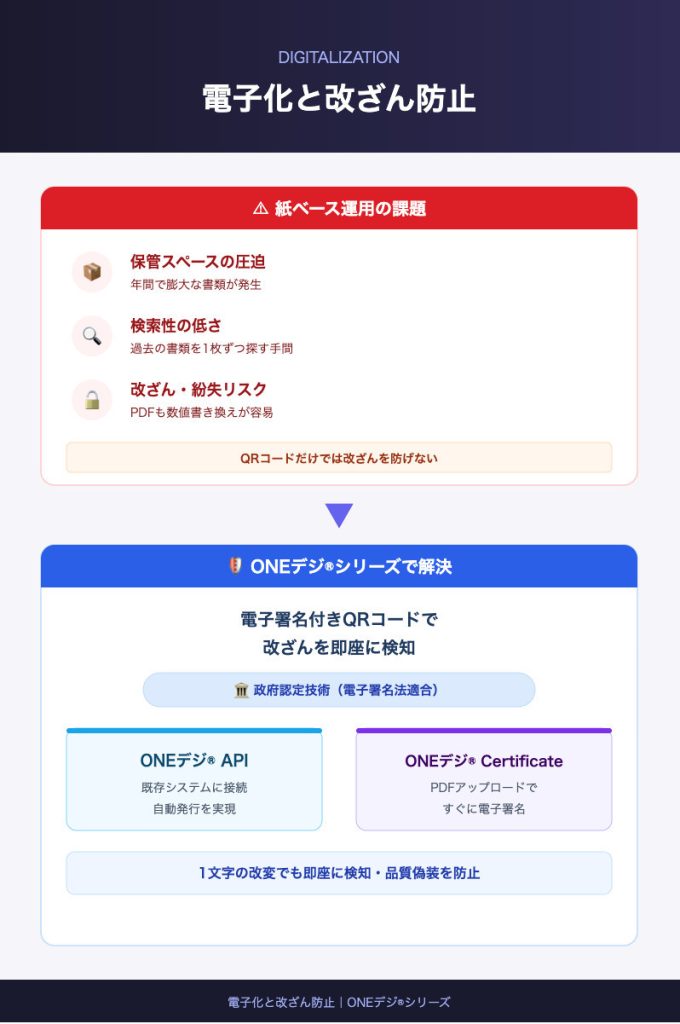
ただし、電子化にあたって見落としてはならないのが、電子データの改ざん防止です。PDFの検査成績書は数値の書き換えが容易であり、単にデジタル化しただけでは紙以上に改ざんリスクが高まる可能性があります。既存のQRコード付きサービスも登場していますが、単にQRコードが付いているだけでは改ざんを完全に防ぐことはできません。
この課題に対し、Le-Techs株式会社が提供するONEデジ®シリーズは、QRコードに電子署名を付与できる唯一のソリューションです。ONEデジ®基盤技術は、2024年2月29日にグレーゾーン解消制度を通じて、内閣総理大臣をはじめとする5人の大臣から電子署名法第2条第1項への適合が公式に認められた政府認定技術です。1文字でも書き換えられた場合にハッシュ値が変化し、即座に改ざんを検知できるため、検査成績書の真正性を確実に保証します。
既に業務システムをお持ちの企業にはONEデジ®APIがおすすめです。新規システムを開発することなく、自社の既存システムに電子署名機能を接続でき、開発コストを大幅に抑えながら導入できます。検査成績書を自動で発行し、電子署名付きQRコード付き証明書として取引先に提供する運用が実現します。詳しくはこちらをご覧ください。
すぐに検査成績書の電子化を始めたい企業にはONEデジ®Certificateが最適です。PDFをアップロードするだけで電子署名を付けられるシンプルなサービスで、単独でご利用いただけます。複雑なシステム構築は不要で、QRコード技術により検査成績書の真正性を簡単に確認できます。詳しくはこちらをご覧ください。
検査成績書システム選定のポイント
検査成績書の電子化システムを選定する際は、以下のポイントを確認しましょう。
まず、自社の製造現場に適したフォーマットやワークフローに対応しているかを確認します。検査項目のカスタマイズ性や、計測機器からの自動データ取り込み機能の有無も重要な評価ポイントです。次に、改ざん防止やアクセス制御などのセキュリティ機能が十分に備わっているかを検討します。特に、電子署名やハッシュ値による真正性の証明機能は、取引先からの信頼確保に直結します。
加えて、既存の生産管理システムやERPとの連携が可能か、導入後のサポート体制が充実しているか、コストパフォーマンスは適切かといった点も総合的に評価することが、導入成功の鍵となります。
検査成績書の活用と改善
検査成績書の活用例
検査成績書は単なる品質証明にとどまらず、製造現場の改善活動にも活用できます。検査データを蓄積・分析することで、不良品の発生傾向やばらつきの原因を特定し、工程改善につなげることが可能です。統計的品質管理(SPC)の手法を用いて検査データをチャートで可視化すれば、品質の変動を早期に検知し、予防的な対応が取れるようになります。
また、取引先から検査成績書の提出を求められる場面では、電子署名付きの検査成績書を迅速に発行できる体制を構築しておくことで、納品リードタイムの短縮と取引先の信頼向上を同時に実現できます。複数の取引先に異なるフォーマットで検査成績書を提出する必要がある場合も、電子化されたシステムであればテンプレートの切り替えで効率的に対応可能です。
現場改善に役立つ資料やセミナー情報
検査成績書の運用改善や電子化の推進にあたっては、製造業向けのセミナーや業界団体が提供する資料を活用することも有効です。品質管理に関する専門家の知見を得ることで、自社に適した運用方法を見つけやすくなります。
なお、検査成績書の運用では実際にさまざまなトラブルが発生します。よくあるケースとしては、検査データの転記ミスによる納品先からのクレーム、保管書類の紛失によるトレーサビリティの断絶、システム移行時のデータ消失などが挙げられます。これらのリスクに対しては、入力時のダブルチェック体制の構築、電子データのバックアップ運用、移行計画の段階的な実施といった対策を事前に講じておくことが重要です。電子署名による改ざん検知機能を備えたシステムを導入することで、こうしたリスクの多くを根本から解消できます。
よくある質問(FAQ)
Q. 検査成績書の保存期間はどれくらいですか? A. 法令上の統一的な保存期間の規定はありませんが、品質マネジメントシステム(ISO 9001等)では一般的に5年〜10年程度の保存が求められます。業界や取引先の要求事項によって異なるため、自社の規定を確認しましょう。
Q. 検査成績書とミルシートは同じものですか? A. いいえ、異なります。ミルシートは材料メーカーが発行する材料の品質証明書であり、検査成績書は完成した製品・部品の検査結果を記録する書類です。
Q. 検査成績書の電子化で改ざんは防げますか? A. 単にPDF化しただけでは改ざん防止にはなりません。電子署名やハッシュ値による真正性の証明機能を備えたソリューションの導入が必要です。ONEデジ®シリーズは、QRコードに電子署名を付与できる唯一の技術であり、1文字でも改変があれば即座に検知できます。
Q. 小規模な企業でも電子化は可能ですか? A. はい。ONEデジ®CertificateはPDFをアップロードするだけで電子署名を付与できるサービスで、単独で利用可能です。大規模なシステム構築は不要なため、小規模な企業でもすぐに導入を始められます。
Q. 既存の生産管理システムと連携して電子署名を付けることはできますか? A. はい。ONEデジ®APIを利用すれば、自社の既存システムに電子署名機能を接続でき、新規にシステムを開発する必要はありません。検査成績書の発行から電子署名付きQRコードの付与までを自動化し、開発コストを抑えながら導入できます。
まとめ
検査成績書は、製品の品質を客観的に証明し、取引先との信頼関係やトレーサビリティを支える製造業の基本書類です。記載内容の正確性はもちろん、作成・管理方法の効率化が品質管理体制全体の向上につながります。
紙ベースの運用には保管スペース、検索性、紛失・劣化、改ざんといった多くの課題があり、電子化の推進が急務です。ただし、電子化にあたっては改ざん防止の仕組みが不可欠です。
ONEデジ®シリーズは、政府認定技術を活用したONEデジ®基盤技術による電子署名付きQRコードで、検査成績書の真正性を法的に証明できる唯一のソリューションです。既存システムへの接続で開発コストを抑えたい企業にはONEデジ®API、すぐに電子署名の運用を始めたい企業にはONEデジ®Certificateをぜひご検討ください。検査成績書の電子化と改ざん防止を同時に実現し、品質管理体制のさらなる強化にお役立ていただけます。
関連記事
DX・業務効率化の全体像を知りたい方はこちら
合わせて読みたい

